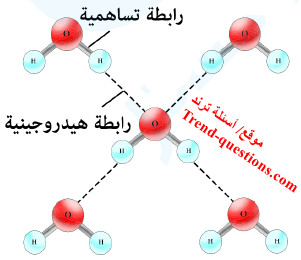
قطبية الماء
- لدراسة قطبية الماء لابد من معرفة المفاهيم التالية أولاً:
- المركب القطبي: هو مركب تساهمي الفرق في السالبية الكهربية بين عنصريه كبير نسبيا.
- السالبية الكهربية: هي مقدرة الذرة في الجزيء على جذب إلكترونات الرابطة الكيميائية نحوها.
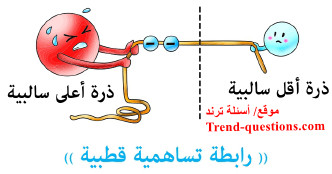
تفسير قطبية الماء
- ترجع قطبية الماء إلي أن ذرة الأكسجين تتميز بارتفاع سالبتيها الكهربية عن ذرة الهيدروجين، ولذلك تنجذب إلكترونات الروابط نحو ذرة الأكسجين بشكل أكبر من ذرتي الهيدروجين فيتكون على ذرة الأكسجين شحنتان سالبتان جزئيتان (-δ) وعلى كل ذرة هيدروجين شحنة موجبة جزئية (+δ)
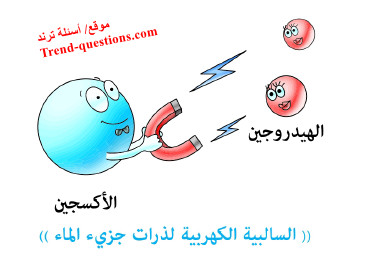
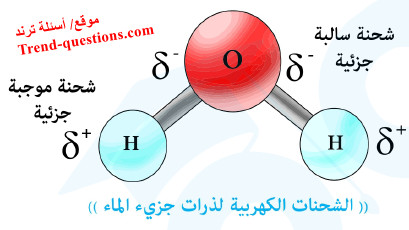
التأثير الناتج عن قطبية الماء
- يترتب على قطبية الماء ما يلي:
مثال : ذوبان ملح كلوريد الصوديوم (ملح الطعام) في الماء.
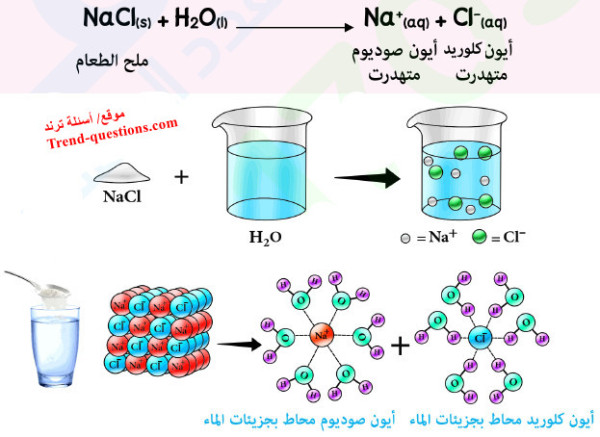
تأثير الروابط الهيدروجينية على خواص الماء
- تعد الروابط الهيدروجينية الموجودة بين جزيئات الماء من أهم العوامل المسئولة عن شذوذ خواص الماء، حيث تسبب ارتفاع درجة غليان الماء النقي تحت الضغط الجوي المعتاد مقارنة بدرجة غليان المركبات المماثلة له في التركيب كما يتضح من الجدول التالي:
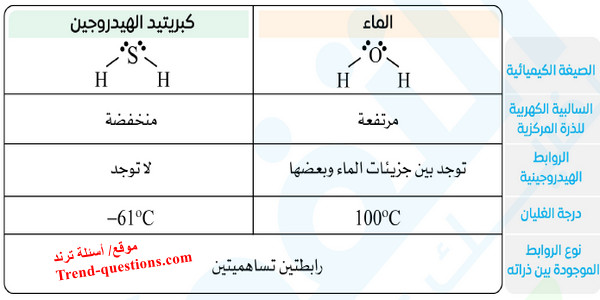
معلومات هامة عن قطبية الماء
(1) لا يوجد الماء على سطح الأرض في صورة نقية حيث يحتوي على العديد من الأيونات، والمواد الكيميائية التي تتفاعل معه بطرق مختلفة.
(2) يعبر عن الحالة الفيزيائية للمادة في معادلات التفاعل الكيميائي بالرموز التالية :
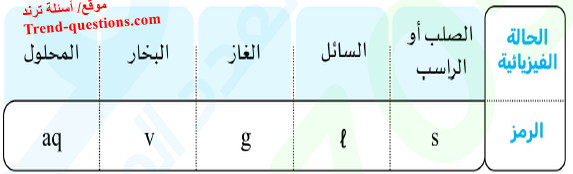
(3) الروابط الهيدروجينية : نوع من التجاذب الإلكتروستاتيكي الضعيف ينشأ بين جزيئات بعض المركبات القطبية نتيجة وقوع ذرة الهيدروجين بين ذرتين مرتفعتين في السالبية الكهربية مثل الأكسجين.
(4) نوع الروابط الموجودة بين الذرات في جزيء الماء روابط تساهمية ، بينما نوع الروابط الموجودة بين جزيئات الماء وبعضها روابط هيدروجينية.
(5) الروابط الهيدروجينية الموجودة بين جزيئات الماء أضعف من الروابط التساهمية الموجودة بين ذرات جزيئات الماء.
(6) يمكن لجزيء الماء الواحد أن يرتبط بأربع جزيئات ماء أخري عن طريق الروابط الهيدروجينية ، نتيجة لوجود (2 شحنة موجبة جزئية + 2 شحنة سالبة جزئية)